
JEDYNE W POLSCE ROZWIĄZANIE**
UNIKATOWE POŁĄCZNIE DWÓCH
NAJLEPIEJ UDOKUMETOWANYCH
SZCZEPÓW BAKTERII
W JEDNEJ PASTYLCE!
MIKROBIOTA
Organizm człowieka zasiedlają miliardy mikroorganizmów tworząc mikrobiotę. Jej skład jest bardzo zróżnicowany w zależności od miejsca występowania. Mikrobiota jamy ustnej oraz nosowo-gardłowej różni się w znaczący sposób od składu mikrobioty jelit pod względem składu gatunkowego bakterii.
Aby organizm funkcjonował prawidłowo wszystkie mikroorganizmy powinny żyć ze sobą w ścisłej równowadze.
O mikrobiotę należy szczególnie zadbać w trakcie stosowania antybiotyku.
W czasie stosowania antybiotyku ważne jest nie tylko wspieranie mikrobioty jelit, lecz równie ważne jest wspieranie mikrobioty jamy ustnej i nosowo-gardłowej, tak aby w całym układzie pokarmowym, na każdym jego etapie panowała równowaga mikrobiotyczna.
W tym celu warto rozważyć stosowanie konkretnych szczepów bakterii, które są aktywne w obrębie jelit oraz w obrębie jamy ustnej i nosowo-gardłowej.
ORYGINALNE UNIKATOWE POŁĄCZENIE JUŻ DOSTĘPNE W POLSCE!
ENTitis® biotyk to JEDYNY w Polsce produkt zawierający BIOTYK COMPLEX, czyli unikatowe połączenie dwóch wyjątkowych szczepów bakterii:
- Streptococcus salivarius K12® w formule Bactoblis®, który jest aktywny w jamie ustnej i nosowo-gardłowej
oraz - Lactobacillus rhamnosus (LGG®) by Chr.Hansen, aktywny w obrębie jelit.
Te dwa różne szczepy działają w dwóch różnych obszarach naszego organizmu, gdzie efektywnie kolonizują i wzmacniają dwa różne mikrobiomy.

DO STOSOWANIA W TRAKCIE ANTYBIOTYKOTERAPII


Dlaczego ENTitis biotyk
do antybiotyku?
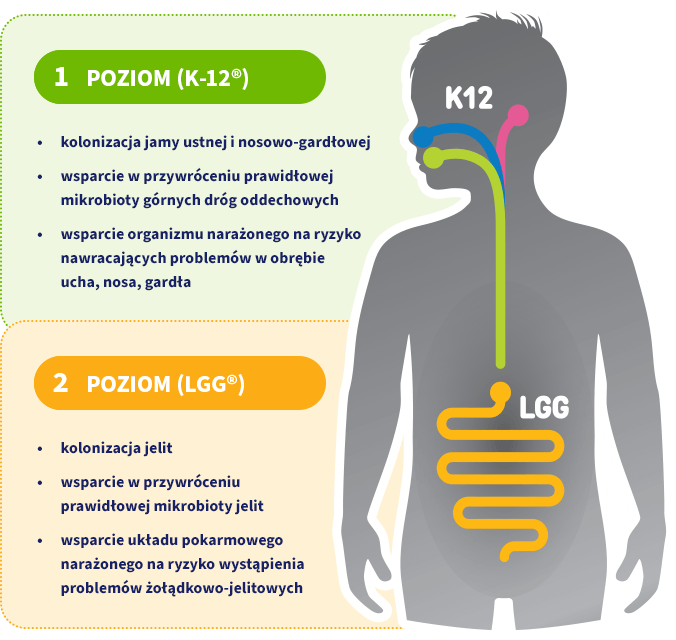
DZIAŁANIE NA DWÓCH POZIOMACH W CZTERECH RÓŻNYCH OBSZARACH ORGANIZMU
Innowacyjna kombinacja dwóch szczepów bakterii wspierająca mikrobiotę zarówno jelit, jak i ucha, nosa, gardła, w tym jamy ustnej.
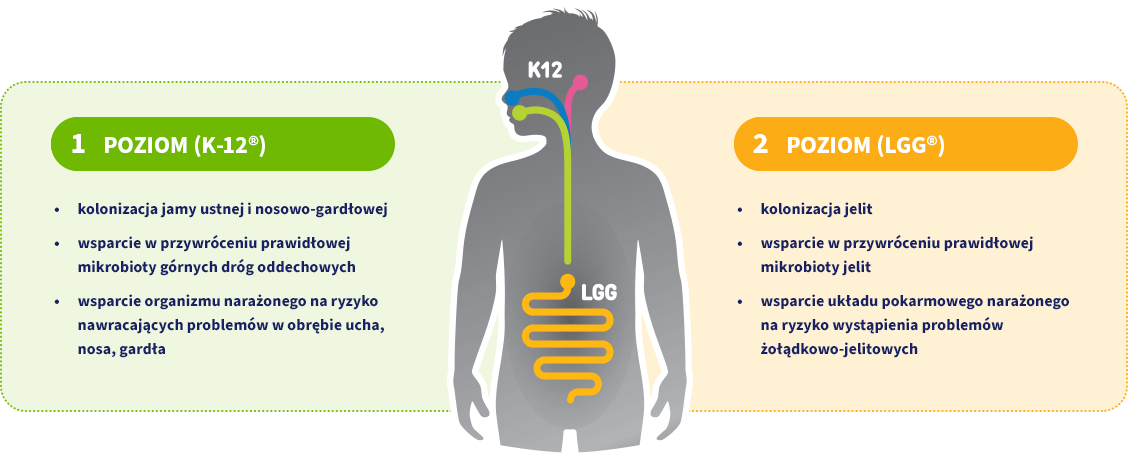
ORYGINALNE, UNIKATOWE
FORMUŁY
Ponad 300 badań nauowych***
Jakość szczepów wykorzystywanych w produktach ma bardzo duże znaczenie, wpływa na stopień kolonizacji mikrobioty, a tym samym na działanie w organizmie. Warto wybierać takie produkty, których oryginalne formuły zostały przebadane w wartościowych badaniach naukowych. Najwyższa jakość oraz oryginalne complexy przekładają się na właściwe działanie. Tylko ENTitis® biotyk zawiera szczepy zamknięte w unikatowych formułach potwierdzonych w ponad 300 badaniach naukowych.

Oryginalna formuła Bctoblis®, w której zamknięty jest szczep K-12®, zapewnia odpowiednią kolonizację jamy ustnej i nosowo-gardłowej.

Oryginalny LGG® by Chr. Hansen zapewnia wysoką jakość szczepu bakterii, jego stabilność genetyczną oraz wysoki stopień przylegania do błony śluzowej jelit.
1 pastylka do ssania zawiera łącznie 6 miliardów żywych kultur bakterii Streptococcus salivarius K-12® oraz Lactobacillus rhamnosus (LGG®).
LGG by Chr. Hansen – poznaj siłę pilusów
„Pilusy” to wypustki bakteryjne przypominające włoski. Zapewniają wysoki stopień przylegania do błony śluzowej.
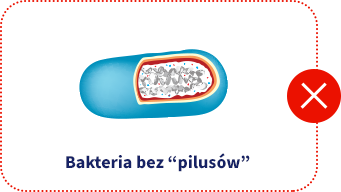
Wiele szczepów bakterii z czasem ulega zmianom, przez co cząsteczki bakterii tracą „pilusy”, co uniemożliwia skuteczne przyleganie do błony śluzowej jelit.
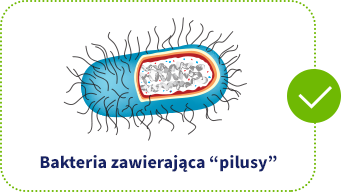
LGG® by Chr. Hansen to wyposażony w „pilusy” szczep, który dzięki zastosowaniu specjalnego procesu produkcyjnego zapewnia stabilność genetyczną, dzięki której zachowuje zdolność skutecznego przylegania do błony śluzowej jelit.
Szczep K-12 w formule Bactoblis® oraz LGG® by Chr. Hansen to efekt zaskakujących odkryć naukowców

Historia szczepu K12 w formule Bactoblis®

Ponad 30 lat temu prof. mikrobiologii John Tagg z Nowej Zelandii dokonał niezwykłego odkrycia. W trakcie badań spostrzegł, że jeden chłopiec jest wyjątkowo odporny. Zaczął szukać odpowiedzi na pytanie ‒ dlaczego? I okazało się, że w jamie ustnej chłopca kryje się szczep K-12. Okazuje się, że ten wyjątkowy szczep ma w sobie jedynie 2% ludzi na świecie. Wiele lat trwało stworzenie specjalnej formuły produktu, w której szczep K-12 zachowa swoje wyjątkowe właściwości. Tak powstała formuła Bactoblis®.
Historia szczepu LGG® by Chr. Hansen
Oryginalny szczep L. rhamnosus (LGG) został wyizolowany z mikroflory ludzkiego jelita przez dwóch naukowców: Gorbacha i Goldina w 1985 roku. Christian Hansen to duński mikrobiolog, któremu udało się wyodrębnić szczep L. rhamnosus (LGG) i stworzyć niezmienną genetycznie formułę, a jego właściwości zostały potwierdzone w blisko 300 badaniach naukowych. Szczep LGG® by Chr. Hansen to najlepiej przebadany szczep probiotyczny na świecie.
Zastosowanie
ENTitis® biotyk jest polecany dla wszystkich dzieci powyżej 3. roku życia i dorosłych, a w szczególności w trakcie antybiotykoterapii, w celu uzupełnienia mikrobioty jamy ustnej, nosowo-gardłowej oraz jelit.
Większość dostępnych produktów probiotycznych stosowanych w trakcie antybiotykoterapii zawiera szczepy bakterii działających wyłącznie w obrębie jelit. Podczas stosowania antybiotyku bardzo ważne jest nie tylko wspieranie mikrobioty jelit, lecz również ważne jest wspieranie mikrobioty jamy ustnej i nosowo-gardłowej. Zapewnienie równowagi mikrobiotycznej w obrębie tych dwóch obszarów jest kluczowe w sytuacji, kiedy zastosowanie antybiotyku jest konieczne.
W jaki sposób działa BIOTYK COMPLEX zawarty w ENTitis® biotyk?
Wielokrotnie przebadany szczep K-12® w formule Bactoblis® oraz LGG® to szczepy aktywnie działające w dwóch różnych obszarach organizmu. Szczep K-12® jest aktywny w górnych drogach oddechowych, kolonizuje jamę ustną i nosowo-gardłową. Szczep LGG® jest aktywny w dalszych odcinkach przewodu pokarmowego, kolonizuje jelita. Szczepy działają niezależnie względem siebie wspierając mikrobiom organizmu.
Zalecane spożycie
- 1 pastylka dziennie
- Pastylkę należy przyjmować przed snem, po umyciu zębów. Pastylkę należy ssać powoli przez ok. 5 minut aż do całkowitego rozpuszczenia. Pastylki nie należy rozgryzać ani połykać.
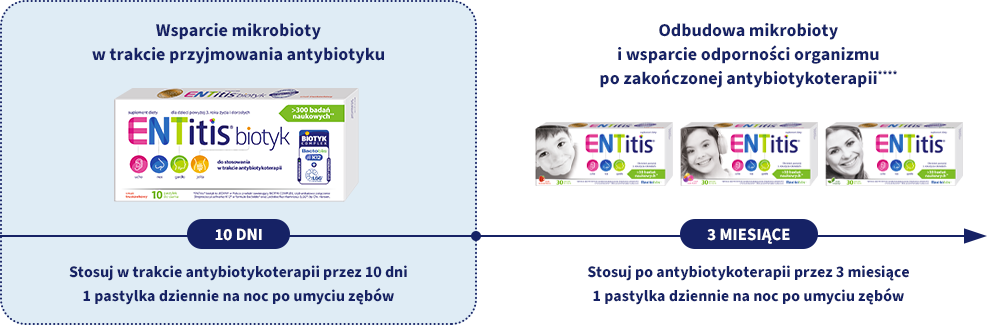
Jak stosować produkt ENTitis® biotyk?
Po zakończonej antybiotykoterapii polecamy 3-miesięczne stosowanie klasycznej formy produktu ENTitis®:
- Dla dzieci powyżej 3. roku życia: ENTitis® w pastylkach do ssania smak truskawkowy lub tutti frutti
- Dla dorosłych: ENTitis® w pastylkach do ssania o smaku miętowym.

** ENTitis biotyk to JEDYNY w POLSCE produkt zawierający taki BIOTYK COMPLEX, czyli unikatowe połączenie Streptococcus salivarius (K-12®) w formule Bactoblis® oraz Lactobacillus rhamnosus (LGG®) by Chr. Hansen.
*** łącznie dla szczepów K12® i LGG®; wykaz badań:
1. Carucci L., et al. Pediatr Allergy Immunol. 2022 Aug;33(8):e13836. 2. Damholt, A., et al (2022). Beneficial Microbes, 13(1), 13–23. 3. Groele L, et al. MJ Open Diabetes Res Care. 2021 Mar;9(1):e001523. 4. Adams CB, et al. BMC Pediatr. 2021 Jul 21;21(1):323. 5. Schnadower D, et al. J Nutr. 2021 Jan 4;151(1):65-72. 6. Mutlu M, et al. Am J Perinatol. 2020 Sep;37(11):1173-1176. 7. Hui, Y., et al (2021). Gut Microbes, 13(1). 8. Forster, C. S., et al. Forster, C. S., et al. 9. Schnadower, D., et al. Pediatr Gastroenterol Nutr, Aug 14 (2020). 10. Larnkjær, A., et al. Pediatric Research, (January), 1–6 (2020). 11. Castro-Mejía, J. L., et al. Gut Microbes, 00(00), 1–13 (2020). 12. Dawe, J. P., et al. Scientific Reports, 10(1), 1–11 (2020). 13. Groah et al. Therapeutic Advances in Urology, 11, 1–13, (2019). 14. Paparo et al, Scientific Reports, 9(1), 1–10, (2019). 15. Schmidt et al. Pediatr Allergy Immunol, 30(3), 1–6, (2019). 16. Bianchini et al. Human Vaccines & Immunotherapeutics, 0(00), 1–9, (2019). 17. Nabukeera-Barungi et al. Paediatrics and International Child Health, 39(2), 95–103, (2019). 18. Adler Sørensen et al. Clinical Microbiology and Infection, 25(4), 511.e1-511.e7, (2019). 19. Cabana et al. Journal of pediatric gastroenterology and nutrition, (2018). 20. Fjeldhøj et al. Scientific Reports, 8(1), 1–9, (2018). 21. Korpela et al. Microbiome, 6(1), 182, (2018). 22. Kallio et al. Clinical & Experimental Allergy. 2018. October. 23. Simpson et al. Journal of Dairy Science, 101(2), 889–899, (2018). 24. Kane et al. J Pediatr. 2018 Apr;195:73-79. 25. Berni Canani et al. Scientific Reports 8.1 (2018). 26. Lazarus et al. Vaccine, Jan 4;36(2):273-279, (2018). 27. Durack et al. Communications 9.1 (2018). 28. Schei, Kasper et al. Microbiome 5.1 (2017). 29. Narbona-López et al. British Journal of Nutrition, 117(7), 994 (2017). 30. Laursen et al. Pediatrics, 140(2), (2017). 31. Berni Canani et al. Allergy Clin Immunol. 2017 Jun;139(6):1906-1913. 32. Lundelin, et al. Pediatric Allergy and Immunology, 28(2), 170–175 (2017). 33. Grenov, et al. Journal of Pediatric Gastroenterology and Nutrition, 64(3), 396–403, (2017). 34. Cabana et al. Pediatrics. 2017 Sep;140(3). 35. Laursen et al. BMC Microbiol. 2017 Aug 17;17(1):175. 36. Rø et al. Clin Exp Allergy. 2017 Aug;47(8):1014-1021. 37. Groele et al. Open 7.10 (2017). 38. Peldan et al. Clinical & Experimental Allergy, 47(7), 975–979, (2017). 39. Scalabrin et al. Eur J Pediatr. 2017 Feb;176(2):217-224. 40. Schnadower et al. BMJ Open, 7(9), 1, (2017). 41. Fatheree, et al. World Journal of Gastrointestinal Pathophysiology, 7(1), 160. (2016). 42. Okesene-Gafa, et al. BMC Pregnancy Childbirth, 16(1):373 (2016). 43. Korpela et al. PLoS ONE, 11(4), 1–16, (2016). 44. Bruzzese, et al. Aliment.Pharmacol.Ther. 2016;44(6):568-575. 45. Okesene-Gafa, et al. BMC Pregnancy Childbirth, 16(1):373 (2016). 46. Fox, et al. BMJ Open 2015;5:1-6. 47. Ovcinnikova, et al. Clinicoecon Outcomes Res. 2015;7:145-152. 48. Dotterud, et al. J.Pediatr.Gastroenterol.Nutr. 2015;61(2):200-207. 49. Berni Canani, et al. Clin.Epigenetics 2015;7(1):38-015-0070-8. eCollection 2015. 50. Pärtty, et al. Pediatric Research, 78(4), 470–475, (2015). 51. Simpson, et al. BMC Dermatology, 15(1), 1–9, (2015). 52. Guest, et al. Clinicoecon Outcomes Res. 2015;7:583-591. 53. Berni Canani, et al. The ISME Journal, 10(3), 742–750, (2015). 54. Pärtty, et al. Pediatr Res, 77(6), 823–828, (2015). 55. Swanljung, et al. Acta Otolaryngol. 2015;135(8):824-830. 56. Aggarwal, et al. Indian J.Med.Res. 2014;139(3):379-385. 57. Luoto, et al. J.Allergy Clin.Immunol. 2014;133(2):405-413. 58. Sindhu, et al. Clin.Infect.Dis. 2014;58(8):1107-1115. 59. Tapiovaara, et al. Int.J.Pediatr.Otorhinolaryngol. 2014;78(10):1637-1641. 60. Havranek, et al. of Perinatology, 33(1), 40–44, (2013). 61. Kumpu, et al. J.Med.Virol. 2013;85(9):1632-1638. 62. Pärtty, et al. J.Pediatr. 2013;163(5):1272-1277.e2. 63. Berni Canani, et al. J.Pediatr. 2013;163(3):771-777. 64. Nylund et al. BMC Microbiology, 13, 12, (2013). 65. Glavina, et al. Antropol. 2012;36(1):129-132. 66. Hoppu, et al. Eur.J.Nutr. 2012;51(2):211-219. 67. Ou, et al. Clin.Exp.Allergy 2012;42(9):1386-. 68. Al-Hosni, et al. J.Perinatol. 2012:253-259.69. Pärtty, et al. PLoS One 2012;7(3):e32495-e32495. 70. Rautava, et al. Placebo-Controlled Trial Neonatology 2012;102(3):178-184. 71. Chrzanowska-Liszewska, et al. Early Hum Dev. 2012;88(1):57-60. 72. Nixon, et al. Pediatr.Emerg.Care 2012;28(10):1048-1051. 73. Kumpu, et al. European Journal of Clinical Nutrition, 66(9), 1020–1023, (2012). 74. Lehtoranta, et al. Int.J.Pediatr.Otorhinolaryngol. 2012;76:206-211. 75. Muraro, et al. BMJ Open 2012;2(2):e000637-. 76. Canani et al. Journal of Allergy and Clinical Immunology, 129(2), (2012). 77. Luoto, et al. Early Hum.Dev. 2012;88(6):339-344. 78. Grönlund, M. M., Grzeskowiak, Ł., Isolauri, E., & Salminen, S. (2011). Gut Microbes, 2(4). 79. Aaltonen, et al. Eur.J.Clin.Nutr. 2011;65:10-19. 80. Myhre, et al. Am.J.Clin.Nutr. 2011;93(8):151-157. 81. Rose, et al. Clin.Exp.Allergy 2011;41(12):1819-1821. 82. Ilmonen, et al. Clin.Nutr. 2011;30(2):156-164. 83. Nermes, et al. Clinical and Experimental Allergy, 41(3), 370–377, (2011). 84. McFarland et al. Education and Practice, 96(6), 238–238. (2010). 85. Cox, et al. PLoS One 2010:e8745. 86. Hojsak, et al. Pediatrics 2010;125:e1171. 87. Hojsak, et al. Clin.Nutr. 2010;29:312-316. 88. Baldassarre, et al. J.Pediatr. 2010;156:397-401. 89. Luoto, et al. Int.J.Obes. 2010;34:. 90. Salmi, et al. Pediatr. Allergy Immunol. 2010;21:e401. 91. Luoto et al. Acta Paediatrica, International Journal of Paediatrics, 99(8), 1135–1138, (2010). 92. Ritchie, et al. J.Pediatr.Gastroenterol.Nutr. 2010;50:619-624. 93. Dotterud, et al. Br.J.Dermatol. 2010;163:616-623. 94. Rose, et al. Clin.Exp.Allergy 2010;40:. 95. Luoto, et al. Br.J.Nutr. 2010;103(12):1792-1799. 96. Underwood et al. Journal of Pediatrics, The, 48(2), 216–225; (2009). 97. Rouge, et al. Am.J.Clin.Nutr. 2009;89:1828-1835. 98. Kuitunen, et al. J.Pediatr.Gastroenterol.Nutr. 2009;49:626-630. 99. Rautava, et al. Br.J.Nutr. 2009;101(11):1722-1726. 100. Kuitunen, et al. Journal of Allergy and Clinical Immunology, 123(2), 335–341 (2009). 101. Scalabrin, et al. Clin.Pediatr. 2009;48:734-744. 102. Aaltonen, et al. J.Pediatr. 2008;152:79-84. 103. Sentongo, et al. J.Pediatr.Gastroenterol.Nutr. 2008;46:41-47. 104. Marschan, et al. Clin.Exp.Allergy 2008;38:611-618. 105. Piirainen, et al. Ann.Nutr.Metab. 2008;52:204-208. 106. Kukkonen, et al. Pediatrics, 122(1), 8–12, (2008). 107. Huurre, et al. Clin.Exp.Allergy 2008;38:1342-1348. 108. Kloster Smerud, et al. Microb.Ecol.Health Dis. 2008;20:80-85. 109. Marschan, et al. Pediatr.Allergy Immunol. 2008;19:132-139. 110. Pediatr.Allergy Immunol. 2008;19:132-139. 111. Mentula, et al. Microb.Ecol.Health Dis. 2008;20(1):37-47. 112. Piirainen, et al. Ann.Allergy Asthma Immunol. 2008;100:338-342. 113. Kaplas, et al. Lipids 2007;42:865-870. 114. Grüber, et al. Allergy 2007;62(11):1270-1276. 115. Bruzzese, et al. Clin.Nutr. 2007;26:322-328. 116. Grönlund, et al. Clin.Exp.Allergy 2007;37(3):1764-1772. 117. Hatakka, et al. Clin.Nutr. 2007;26:314-321. 118. Kukkonen, et al. J.Allergy Clin.Immunol. 2007;119:192-198. 119. Honeycutt, et al. Pediatric Critical Care Medicine, 8(5), 452–458, (2007). 120. Kalliomäki et al. Journal of Allergy and Clinical Immunology, 119(4), 1018–1019; (2007). 121. Gueimonde, et al. J.Pediatr.Gastroenterol.Nutr. 2006;42:166-170. 122. Rinne, et al. J.Pediatr.Gastroenterol.Nutr. 2006;43:200-205. 123. Gueimonde, et al. J.Pediatr.Gastroenterol.Nutr. 2006;42:604-606. 124. Rautava, et al. Pediatr.Res. 2006;60:221-224. 125. Vendt, et al. J.Hum.Nutr.Diet. 2006;19:51-58. 126. Galpin, et al. Am.J.Clin.Nutr. 2005;82:1040-1045. 127. Viljanen, et al. Allergy 2005;60:494-500. 128. Bousvaros, et al. Inflamm.Bowel Dis. 2005;11:833-839. 129. Petschow, et al. J.Clin.Gastroenterol. 2005;39:786-790. 130. Laitinen, et al. Br.J.Nutr. 2005;94:565-574. 131. Bausserman, Michail. J.Pediatr. 2005;147:197-201. 132. Viljanen, et al. Pediatr.Allergy Immunol. 2005;16:65-71. 133. Rinne, et al. J.Pediatr. 2005;147:186-191. 134. Viljanen, et al. Allergy Clin.Immunol. 2005;115:1254-1259. 135. Schultz, et al. J.Pediatr.Gastroenterol.Nutr. 2004;38:293-297. 136. Salazar-Lindo, et al. BMC Pediatrics, 4(1), 1–9, 2004. 137. Pohjavuori, et al. J.Allergy Clin.Immunol. 2004;114:131-136. 138. Agarwal, et al. J.Pediatr.Gastroenterol.Nutr. 2003;36:397-402. 139. Kirjavainen, et al. Journal of Pediatric Gastroenterology and Nutrition, 36(2), 223–227; 2003. 140. Costa-Ribeiro, et al. J.Pediatr.Gastroenterol.Nutr. 2003;36:112-115. 141. Kalliomaki, et al. Lancet 2003;361:1869-1871. 142. Rautava et al. J Allergy Clin Immunol 2002;109:119-21. 143. Helin, et al. Allergy 2002;57:243-246. 144. Rautava, et al. J.Allergy Clin.Immunol. 2002;109:119-121. 145. Kankaanpää, P. E., Yang, B., Kallio, H. P., Isolauri, E., & Salminen, S. J. (2002). The Journal of nutritional biochemistry, 13(6), 364–369. 146. Hatakka, et al. BMJ 2001;322(7298):1327. 147. Näse, et al. Caries Res. 2001;35(6):412-420. 148. Kalliomaki, et al. Lancet 2001;357(9262):1076-1079. 149. Gupta, et al. J.Pediatr.Gastroenterol.Nutr. 2000;31:453-457. 150. Isolauri, et al. Clin.Exp.Allergy 2000;30(11):1604-1610. 151. Pessi, et al. Clin.Exp.Allergy 2000;30(12):1804-1808. 152. Vanderhoof, et al. West.J.Med. 2000;173:397. 153. Oberhelman, et al. J.Pediatr. 1999;134:15-20. 154. Arvola, et al. Pediatrics 1999;104:e64. 155. Vanderhoof, et al. J.Pediatr. 1999;135:564-568. 156. Rautanen, et al. Arch.Dis.Child. 1998;79:157-160. 157. Majamaa, Isolauri. J.Allergy Clin.Immunol. 1997;99:179-185. 158. Shornikova, et al. Acta Paediatr. 1997;86:460-465. 159. Gronlund, et al. Acta Paediatr, 86(4), 440–441, (1997). 160. Malin, et al. Inflammopharmacology 1997:219-236. 161. Malin, et al. Br.J.Rheumatol. 1996;35:689-694. 162. Malin, et al. Ann.Nutr.Metab. 1996;40:137-145. 163. Isolauri, et al. Vaccine 1995;13:310-312. 164. Majamaa, et al. J.Pediatr.Gastroenterol.Nutr. 1995;20:333-338. 165. Kaila, et al. Arch.Dis.Child. 1995;72:51-53. 166. Isolauri, et al. Dig.Dis.Sci. 1994;39(12):2595-2600. 167. Stansbridge, et al. Arch.Dis.Child. 1993;69:488-492. 168. Millar, et al. Arch.Dis.Child. 1993;69:483-487. 169. Kaila, et al. Pediatr.Res. 1992;32:141-144. 170. Isolauri, et al. Pediatrics 1991;88:90-97. 171. Oksanen, et al. Ann.Med. 1990;22:53-56. 172. Aljumaah MR., et al. Clin Nutr. 2022 Nov;41(11):2565-2576. 173. Mahboobi S, et al. Front Nutr. 2022 Sep 28;9:1018357. 174. Rauseo AM, et al. Infect Control Hosp Epidemiol. 2022 Feb;43(2):167-173. 175. Tractenberg RE, et al. PM R. 2021 Jul;13(7):695-706. 176. Johnstone, J., et al. JAMA – Journal of the American Medical Association, 326(11), 1024–1033. 177. Castro-Herrera VM, et al. Front Immunol. 2021 Mar 4;12:643321. 178. Forster, C. S., et al. J Spinal Cord Med. 2021 Jan;44(1):62-69. 179. Bornholdt, J., et al. Gut Microbes. 2020 Nov 9;12(1):1-14. 180. Butler, C. C., et al. JAMA – Journal of the American Medical Association, 324(1), 47–56 (2020). 181. Sanborn, V., et al. Diabetes and Metabolic Syndrome: Clinical Research and Reviews, 14(5), 907–909 (2020). 182. Dawe, J. P., et al. Scientific Reports, 10(1), 1–11 (2020). 183. Sanborn, V., Azcarate-Peril, M. A., Updegraff, J., Manderino, L., & Gunstad, J. (2020). Neuropsychiatric disease and treatment, 16, 2765–2777. 184. Toh, S., et al. Spinal Cord, 1–13. (2020). 185. Bianchini et al. Human Vaccines & Immunotherapeutics, 0(00), 1–9, (2019). 186. Okesene-Gafa et al. American Journal of Obstetrics and Gynecology, 221(2), 152.e1-152.e13 (2019). 187. Forster et al. Journal of Spinal Cord Medicine, 0(0), 1–8, (2019). 188. Seppo et al. JAMA Pediatrics, 1–3, (2019). 189. Wang et al. Journal of the American Geriatrics Society, 66(7), 1346–1352, (2018). 190. Simpson et al. Journal of Dairy Science, 101(2), 889–899, (2018). 191. Dickerson et al. Bipolar Disorders, 1–8, (2018). 192. Harata et al. European Journal of Nutrition, 56(7), 2245–2253, (2017). 193. Poutsiaka et al. Journal of Applied Microbiology, 122(5), 1321. (2017). 194. Burton et al. British Journal of Nutrition, 117(9), 1312–1322, (2017). 195. Gorshein et al. International Journal of Laboratory Hematology, 31(5), (2017). 196. Costabile et al. Frontiers in Immunology, 8, 1–13 (2017). 197. Kalima, et al. Beneficial Microbes, 7(4), 463–471, (2016). 198. Gueimonde, et al. Food Funct., 7(3), 1601–1609, (2016). 199. Tapiovaara, et al. International Forum of Allergy and Rhinology, 6(8), 848–853, (2016). 200. Cook, et al. Trials, 17, 377 (2016). 201. Solano-Aguilar, et al. PLoS One 2016;11(2):e0147426. 202. Kolmeder et al. PLoS ONE, 11(4), 1–23, (2016). 203. Doron, et al. Antimicrob.Agents Chemother. 2015;59(8):4593-4599. 204. Kwon, et al. Infect.Control Hosp.Epidemiol. 2015;36(12):1451-1454. 205. Tomasik, et al. Biomarker Insights, 10, 47–54, (2015). 206. Hauser, et al. Medicine (Baltimore) 2015;94(17):e685-. 207. Kumpu, et al. Benef Microbes 2015;6(5):631-639. 208. Eloe-Fadrosh, et al. MBio, 6(2), 1–12, (2015). 209. Hoppu, et al. Nutrition 2014;30(2):159-164. 210. Lehtoranta, et al. J.Clin.Virol. 2014;60(3):276-281. 211. Bajaj, et al. Aliment.Pharmacol.Ther. 2014;39(10):1113-1125. 212. Hibberd, et al. PLoS One 2014;9(12):e113456. 213. Dickerson, et al. Prim.Care.Companion CNS Disord. 2014;16(1):. 214. Smith, et al. Br.J.Nutr. 2013;109(11):1999-2007. 215. Nitert, et al. BMC Pregnancy Childbirth 2013;13:50-2393-13-50. 216. Lahti et al. PeerJ, 2013(1), 1–25. 217. Granata, et al. Int.J.Food Sci.Nutr. 2013;64(2):162-168. 218. Kumpu, et al. Br.J.Nutr. 2013;109(12):2240-6. 219. Välimäki, et al. Int.J.Sports Med. 2012;33(4):291-296. 220. Luoto, et al. Early Hum.Dev. 2012;88(6):339-344. 221. Ou, et al. Clin.Exp.Allergy 2012;42(9):1386-1396. 222. Hoppu, et al. Eur.J.Nutr. 2012;51(2):211-219. 223. West, et al. Gut Microbes 2012;3(3):. 224. van Baarlen, et al. Proceedings of the National Academy of Sciences, 108(Supplement_1), 4562–4569, (2010). 225. Ilmonen, et al. Clin.Nutr. 2011;30(2):156-164. 226. Kubota, et al. Curr.Microbiol. 2010;62. 227. Ferrie et al. Journal of Parenteral and Enteral Nutrition, 35(1), 43–49, (2011). 228. Kekkonen, et al. Journal of Nutrition, 141(5), 870–876, (2011). 229. Davidson, et al. Eur.J.Clin.Nutr. 2011;65(4):501-507. 230. Myhre, et al. Am.J.Clin.Nutr. 2011;93(8):151-157. 231. Frech, et al. Clin.Exp.Rheumatol. 2011;29(2 Suppl 65):S22. 232. Brantsćter, et al. Am.J.Epidemiol. 2011;174(7):807-815. 233. Holma, et al. J.Nutr. 2010;140:534-541. 234. Saxelin, et al. Int.J.Food Microbiol. 2010;144:. 235. Barraud, et al. Intensive Care Med. 2010;36(9):1540-1547. 236. Lyra et al. BMC Gastroenterology, 10, (2010). 237. Morrow, et al. Am.J.Respir.Crit.Care Med. 2010;182:. 238. Dommels, et al. Appl.Environ.Microbiol. 2009;75(19):6198-6204. 239. Kubota, et al. Microbiol.Immunol. 2009;53:198-205. 240. Laitinen, et al. Br.J.Nutr. 2009;101(11):1679-1687. 241. Kawase, et al. Int.J.Food Microbiol. 2009;128:429-434. 242. Kawase, et al. Int.J.Probiotics Prebiotics 2009:241-248. 243. Kekkonen, et al. World J.Gastroenterol. 2008;14(13):2029-2036. 244. Wenus, et al. Eur.J.Clin.Nutr. 2008;62:299-301. 245. Kekkonen, et al. World J.Gastroenterol. 2008;14(20):3188-3194. 246. Piirainen, et al. Ann.Allergy Asthma Immunol. 2008;100:338-342. 247. Osterlund, et al. Br.J.Cancer 2007;97:1028-1034. 248. Kekkonen, et al. Int.J.Sport Nutr.Exerc.Metab. 2007;17:352-363. 249. Hatakka, et al. J.Dent.Res. 2007;86:125-130. 250. Myllyluoma, et al. Dig.Liver Dis. 2007;39:516-523. 251. Cohen, et al. In Vivo 2007;21:507-512. 252. Roller, et al. Br.J.Nutr. 2007;97:676-684. 253. Myllyluoma, et al. Int.J.Antimicrob.Agents 2007;29:66-72. 254. Moreira, et al. Respir.Med. 2007;101:1123-1131. 255. Larkin, et al. Nutrition 2007;23(10):709-718. 256. Rafter, et al. Am.J.Clin.Nutr. 2007;85:488-496. 257. Kekkonen RA, et al. Milchwissenschaft 2007;62:326-330. 258. Manley, et al. Med.J.Aust. 2007;186:454-457. 259. Yli-Knuuttila, et al. Oral Microbiol.Immunol. 2006;21:129-131. 260. Hongisto, et al. Eur.J.Clin.Nutr. 2006;60:319-324. 261. Kajander, Korpela. Asia Pac.J.Clin.Nutr. 2006;15:576-580. 262. Kajander, et al. Aliment.Pharmacol.Ther. 2005;22:387-394. 263. Myllyluoma, et al. Aliment.Pharmacol.Ther. 2005;21(10):1263-1272. 264. Devillard, et al. Infect.Dis.Obstet.Gynecol. 2005;13:25-31. 265. de Vrese, et al. Eur.J.Nutr. 2005;44:406-413. 266. Schultz, et al. BMC Gastroenterology, 4, 3–6, (2004). 267. Salminen, et al. HIV.Clin.Trials 2004:183-191. 268. Gosselink, et al. Dis.Colon Rectum 2004;47:876-884. 269. Hatakka, et al. Scand.J.Rheumatol. 2003;32:211-215. 270. Gluck, Gebbers. Am.J.Clin.Nutr. 2003;77:517-520. 271. Kuisma, et al. Aliment.Pharmacol.Ther. 2003;17:509-515. 272. Colodner, et al. Israel Medical Association Journal, 5(11), 767–769; 2003. 273. Schultz, et al. J.Dairy Res. 2003;70(2):165-173. 274. Helin, et al. Allergy 2002;57:243-246. 275. Ahola, et al. Arch.Oral Biol. 2002;47(11):799-804. 276. Mirasoli, et al. Minerva Gastroenterol.Dietol. 2002;48:45-49. 277. Kontiokari, et al. BMJ 2001;322(7302):1571. 278. Gotteland, et al. Aliment.Pharmacol.Ther. 2001;15:11-17. 279. Apostolou, et al. FEMS Immunol.Med.Microbiol. 2001;30:217-221. 280. Thomas, et al. Mayo Clin.Proc. 2001;76:883-889. 281. Fang, et al. FEMS Immunol.Med.Microbiol. 2000;29:47-52. 282. Alander, et al. Appl.Environ.Microbiol. 1999;65:351-354. 283. Pelto, et al. Clin.Exp.Allergy 1998;28(12):1474-1479. 284. Hilton, et al. J.Travel Med. 1997, 4(1) :41-43. 285. Alander, et al. Lett.Appl.Microbiol. 1997;24:361-364. 286. Bennet, et al. Nutrition today supplemenmt. 1996;31(6):35S-38S. 287. Saxelin, et al. Int.J.Food Microbiol. 1995;25(2):199-203. 288. Ling, et al. J.Nutr. 1994;124:18-23. 289. Meurman, et al. Microb.Ecol.Health Dis. 1994:295-298. 290. Saxelin, et al. Microb.Ecol.Health Dis. 1993:119-122. 291. Goldin, et al. Dig.Dis.Sci. 1992;37:121-128. 292. Ling, et al. Ann.Nutr.Metab. 1992;36:162-166. 293. Saxelin, et al. Microb.Ecol.Health Dis. 1991:209-214. 294. Oksanen, et al. Ann.Med. 1990;22:53-56. 295. Siitonen, et al. Ann.Med. 1990;22:57-59. 296. Gorbach, et al. 1987(8574):1519. 297. Di Pierro F. et al. Int J General Medicine, 2012:5, 991–997. 298. Di Pierro F. et al. Clinical Evaluation: Streptococcus salivarius K12 for Recurrent Pharyngitis Prevention in Adults, 2013, 1-5. 299. Di Pierro F. et al. Drug, Healthcare and Patient Safety, 2014:6, 15–20. 300. Di Pierro F. et al. Int J General Medicine, 2015:8, 303-308. 301. Gregori G. et al. Therapeutics and Clinical Risk Management, 2016:12, 87-92. 302. Di Pierro F. et al. Drug, Healthcare and Patient Safety, 2016:8, 77-81. 303. Di Pierro F. et al. Eur. Rev. Med. Pharm. Sci.,2016:20, 4601-4606. 304. Gun T. Paripex Indian J. Res., 2017, 633-634. 305. Kryuchko T.O., Tkachenko O.Ya., Ukrainian Med. Dent. Acad., Lantibiotics for Preventing Recurrent Upper Respiratory Tract Infections in Children, 2017, 27-32.306. Di Pierro F. et al. Edizioni Minerva Med., 2018, 70(3):240-245. 307. Gavrilenko Yu.V., Prevention of Recurrent Pharyngeal Infections in Children with Antibiotics, 2018, 82-94. 308. Marushko T.V. et al. Streptococcus salivarius K12 in Preventing and Treating Chronic Tonsillitis in Children, 2018, 82-88. 309. Kruchko T.O., Tkachenko O. Ya. Clinical Use of Streptococcus salivarius K12 for Preventing Pharyngotonsillitis and Respiratory Infections in Children, 2018, 122-127. 310. Marini G. et al. Int J General Medicine, 2019:12, 213-217. 311. Havrylenko Yu.V. Clinical Use of Respiratory Probiotic Bactobolis in Children with Secretory Otitis Media, 2019, 90-93. 312. Ilchenko S.I. et al. Pediatrics. Eastern Europe, 2019, 559-565. 313. Bezshapochny S.B. et al. Optional Location Therapy for Chronic Tonsillopharyngitis Remission, Otorhinolaryngology 3(3), 2020, 38-42. 314. Sarlin S. et al.The Pediatr. Infect. Dis. J. 2020;XX:00-00, 1-9. 315. Karakov K. G. et al. Actual problems in dentistry, 2020, 18-21. 316. Kramarev S. O. et al. Actual Infectology, Application of S. salivarius K12 Probiotic in Acute Tonsillopharyngitis Treatment in Children. 2020, 6-11. 317. Ilchenko S.I. et al. Actual Infectology, Efficiency of Respiratory Probiotic S. salivarius K12 in Children with Recurrent Tonsillitis, 2020, 35-39. 318. Kryuchko T.O., Tkachenko O.Ya. Nutrafoods, 2021, 1:246-253. 319. Kryuchko T.O., Tkachenko O.Ya. Nutrafoods, 2021, 2:254-261. 320. Savlevich E.L. et al. Vestnik otorinolaringologii, Vol. 86, No. 6, 2021, 42-47. 321. Puhlik S.M. et al. Experience with Oral Probiotic S. salivarius K12 for Preventing Recurrent Pharyngotonsillar Episodes, 2021, 120-124. 322. Wang Q. et al. Oropharyngeal Probiotic ENT-K12 Prevents Respiratory Tract Infections Among Frontline Medical Staff Fighting Against COVID-19: A Pilot Study, 2021. 323. Di Pierro F. et al. Minerva Medica 2021, 112(4):514-6. 324. Kryuchko T., Tkachenko O. et al. Pediatrics. Eastern Europe, 2021; 9(3), 482-491. 325. Guo H. et al. Oropharyngeal Probiotic ENT-K12 as an Effective Dietary Intervention for Children With Recurrent Respiratory Tract Infections During Cold Season, 2022. 326. Babina K. et al. A Pilot Random. Clinical Trial. Nutrients, 2022, 7;14(5):1124. 327. A.Y. Ovchinnikov et al. Possibilities of probiotic therapy in chronic inflammatory diseases of the oropharynx. Effective pharm. 2022; 18 (4): 24–28. 328. Zangrilli A. et al. Probiotics and Antimicrobial Proteins, 2022, 14:573–578. 329. Di Pierro F. et al. Microorganisms, Clinical Effects of Streptococcus salivarius K12 in Hospitalized COVID-19 Patients: Results of a Preliminary Study 2022; 10(10):1926. 330. La Torre F. et al. Preliminary data revealing efficacy of SSK12 in Periodic Fever, Aphthous stomatitis, Pharyngitis, and cervical Adenitis (PFAPA) syndrome: A multicenter study from the AIDA Network PFAPA syndrome registry, 2023. 331. Bertuccioli A. et al. Use of
**** Właściwości produktu wynikają z działania składników. ENTitis zawiera szczep Streptococcus salivarius K-12® w formule Bactoblis® oraz witaminę D, która pomaga w prawidłowym funkcjonowaniu układu odpornościowego. Bactoblis® jest zarejestrowanym znakiem towarowym Pharmextracta S.P.A. i licencjonowanym wyłącznie przez Bluestone Pharma GmbH. Bactoblis® to produkt w postaci wolno rozpuszczającej się formuły zawierającej nie mniej niż 1 miliard jednostek tworzących kolonię szczepu Streptococcus salivarius K-12®.
LGG® to zarejestrowany znak towarowy Chr. Hansen A/S.



